药物非临床研究质量管理规范(GLP)认证
服务指南
一、适用范围
本指南适用于药物非临床研究质量管理规范(GLP)认证的申请和办理。
二、项目信息
(一)项目名称:药物非临床研究质量管理规范(GLP)认证
(二)事项审查类型: 前审后批
(三)项目编码: 30009
三、办理依据
《药物非临床研究质量管理规范》(国家食品药品监督管理局令第2号)
四、受理机构
国家食品药品监督管理总局食品药品审 核查验中心(简称核查中心)
五、决定机构
国家食品药品监督管理总局
六、审批数量
无数量限制
七、申请条件
申请人条件:从事药物非临床研究的实验室,应建立完善的组织管理体系,配备机构负责人、 质量保证部门负责人和相应的工作人员。
八、申请材料
(一) 申请材料清单
- 药物非临床研究质量管理规范认证申请表;
- 申请机构法人资格证明文件;
- 药物研究机构备案证明文件;
- 机构概要;
- 组织机构的设置与职责;
- 机构人员构成情况、人员基本情况以及参加培训情况;
- 机构主要人员情况;
- 动物饲养区域及动物试验区域情况;
- 检验仪器、仪表、量具、衡器等校验 和分析仪器验证情况;
- 机构主要仪器设备一览表;
- 标准操作规程目录;
- 计算机系统运行和管理情况;
- 药物安全性评价研究实施情况;
- 既往接受GLP和相关检查和整改情况;
- 实施《药物非临床研究质量管理规范》的自查报告;
- 其他有关资料。
(二)对申报资料的一般要求
- 申报资料首页为申报资料项目目录,目录中申报资料项目按照《药物非临床研究质量管理规范认证管理办法》中需要的资料顺序排列,并标明资料的名称或该资料所在目录中的序号。
- 按照《药物非临床研究质量管理规范认证管理办法》附件2要求,以下申报资料应齐全:
(1)《药物非临床研究质量管理规范认证申请表》。
(2)申请机构法人资格证明文件。
企业单位提交企业法人登记证复印件和企业法人营业执照复印件;事业单位提交事 业单位法人登记证复印件和上级主管部门签 发的有效证明文件原件或复印件;其他依法成立的机构提交上级主管部门或具有法人资 格的挂靠单位签发的有效证明文件等复印
件;以上机构均应提交组织机构代码证(副本)复印件。
(3)药物研究机构备案证明文件。
(4)机构概要
- 机构发展概况(包括历史沿革,开展药物安全性评价试验和按GLP开展药物安全性评价试验的基本情况等);
- 组织机构框架图(说明各部门名称、相互关系、各部门负责人等);
- 实验设施平面图(包括整体平面图和外观照片,GLP与非GLP区域平面图,实验 室、动物饲养室、管理区域等平面图及各区 域的面积等)。
(5)组织机构的设置与职责(包括机构 管理部门的设置情况,供试品保管、动物饲养与管理、病理检查及质量保证等部门职能概要)。
(6)机构人员构成情况、人员基本情况以及参加培训情况。
(7)机构主要人员情况(包括机构负责人、质量保证部门负责人、专题负责人、动物饲养管理负责人、组织病理学检查部门负责人、资料保管负责人、供试品管理负责人及其他负责人)。
(8)动物饲养区域及动物试验区域情况。
- 动物设施面积和动物收容能力情况。
- 各动物饲养区的平面图(包括动物饲养设施、 动物用品供给设施、试验操作区、 污物处理区域等)。
- 动物饲养区人流、动物流、物品流、污物流、空气流等流向图(可结合平面图绘制),空气净化系统的送风、回风和排气平面布局图。
- 环境条件,包括动物饲养室的温度、 湿度、压力差、照度、噪声、洁净度、氨浓度等环境条件的控制方法、监控程序或方法以及发生异常时的应急预案;实验动物设施温度、湿度、压力梯度、微生物等环境条件的年度检查报告和检测数据等。
- 饲料、饮水、垫料等动物用品的来源 与检测频次(包括饲料生产厂家、营养学分析、有害物质的分析、卫生学等检测结果以及饮水的检测结果等)。
- 功能实验室、 化学及生物污染特殊区域的环境控制状况。
- 清洁剂、消毒剂、杀虫剂使用情况。
- 实验动物的来源、 质量合格证明和检 疫情况。用于药物非临床安全性评价研究的实验动物应说明来自具有国家统一核发实验动物生产许可证的具体单位名称并提供相关证明资料,检疫情况包括动物种群的近期健康及病原微生物检测结果等。
(9)仪器、仪表、量具、衡器等计量检定情况和分析仪器验证情况。
(10)机构主要仪器设备一览表。
(11)标准操作规程(SOP)目录(包括SOP的制订、修改及废弃的SOP和 SOP标题)。
(12)计算机系统运行和管理情况。
(13)药物安全性评价研究实施情况。
- 药物安全性评价试验实施程序(安全性评价试验流程图);
- 列表说明近三年来开展药物安全性评价试验工作情况(包括按照GLP要求或非GLP条件开展的研究项目的名称、专题负责人姓名、试验起止时间、通过新药审评情况等)。
- 列表说明整改后按照GLP要求开展药物非临床安全性评价工作的情况(仅要求申请整改后复查的机构提供)。
(14)既往接受GLP和相关检查的情况
对于申请整改后复查的机构,应包含前次认证发现问题的整改报告和相关资料,具体说明发现的问题,采取的整改措施和整改 结果等。
(15)实施《药物非临床研究质量管理规范》的自查报告。报告内容应包括自查时 间、参加人员、自查依据、自查内容、自查结果、发现的问题及整改情况等。
(16)其他有关资料。
- 申报资料应使用A4规格纸打印或复印,内容完整、规范、清楚,不得涂改。
- 资料份数:书面资料一份。
- 上述各类复印件均应加盖原件持有单 位公章。
(三)申报资料的具体要求
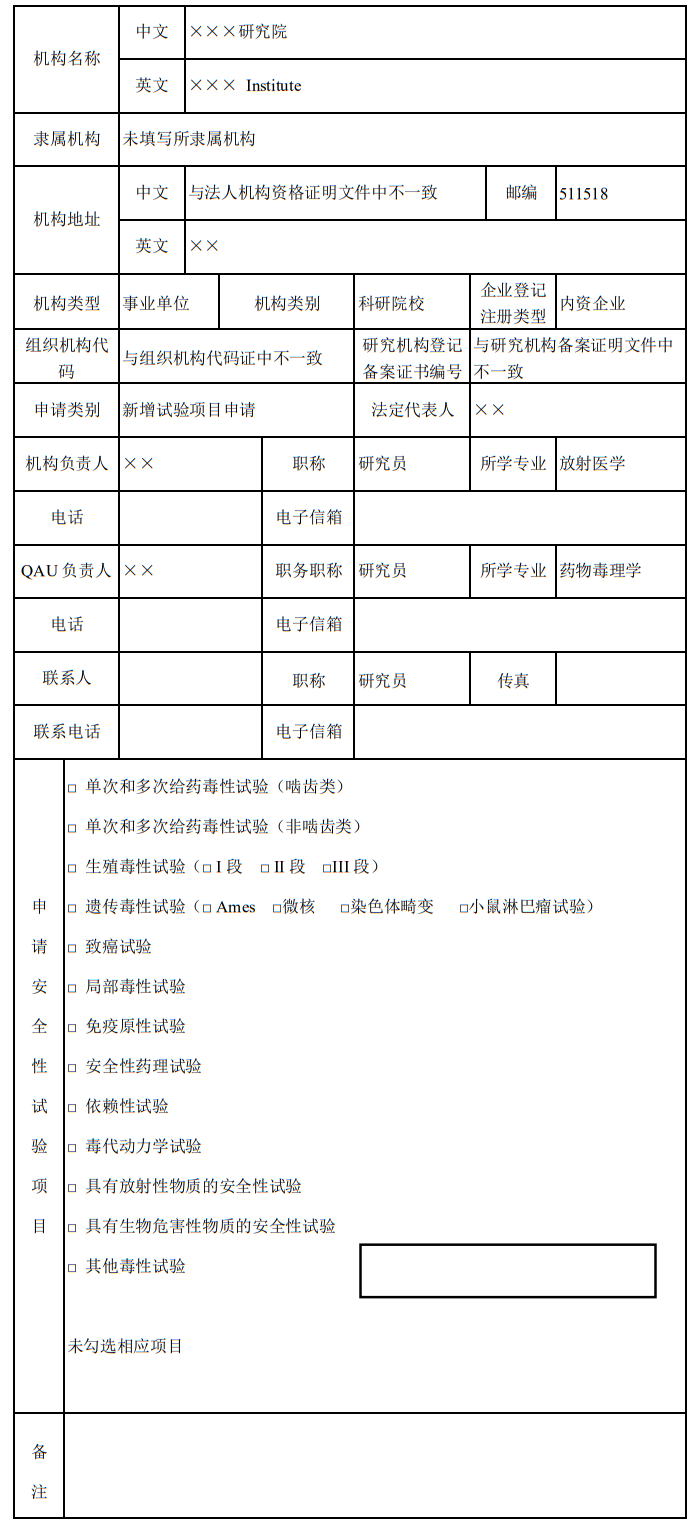
《药物非临床研究质量管理规范认证申请表》是申请人提出药物非临床研究质量管理规范认证的基本文件,应按照填表说明,准确、规范填写:
- 申请表的封面应加盖法人机构公章。
- 非临床研究机构( 实验室) 名称: 应填写法人机构名称,如果需要体现实验室的名称,可将实验室的名称填写在括号内,放置法人机构名称的后面。
- 申请安评试验项目:可在申请表中设置的对应项目中打“√”。
九、申请接收
(一)接收方式
- 电子申请:
国家食品药品监督管理总局网站www.cfda.gov.cn
- 信函接收:
- 接收部门:国家食品药品监督管理总局 食品药品审核查验中心
- 接收地址:北京市西城区宣武门西大街28号大成广场3门一层(总局办公大楼西侧)
- 邮政编码:100053
- 联系电话:010-88331866
- 电子邮箱:cfdi@cfdi.org.cn
(二)对外办公时间
上午9∶00—11∶30
下午13∶00—16∶00
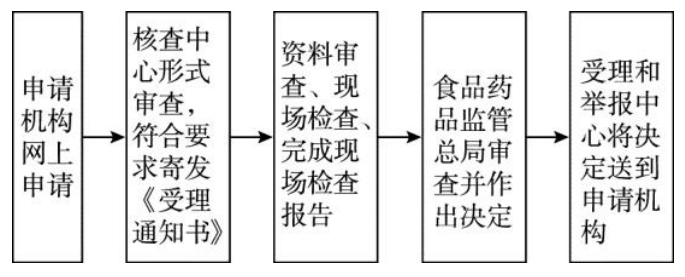
十、办理基本流程
十一、办理方式
(一) 受理
申请机构在国家食品药品监督管理总局网站上登陆药物非临床研究质量管理规范电子申请系统,在线填报申请书和申请资料。电子申请完成后将纸质资料寄至国家食品药品监督管理总局食品药品审核查验中心,5个工作日内进行形式审查,并作出受理决定。
(二) 资料审查与现场检查
- 核查中心进行资料审查和现场检查。
- 核查中心在现场检查结束后完成检查 结果的分析和汇总,向国家食品药品监督管 理总局药品化妆品注册管理司报送现场检查审核件及相关资料。
(三) 审查及决定
国家食品药品监督管理总局在20个工作日内作出审批决定。对通过GLP认证的,发给GLP认证批件,并通过国家食品药品监督管理总局网站予以公告。
十二、审批时限
(一) 受理: 5个工作日。
(二) 行政许可决定:20个工作日(不含现场检查、专家审查和申请人补充资料及补充资料审评所需的时间)。20个工作日内不能作出决定的,经国家食品药品监督管理总局领导批准,可延长10个工作日。
十三、审批收费依据及标准
不收费。
十四、审批结果
许可证件有效期限:3年。
许可年审或年检:无。
十五、结果送达
国家食品药品监督管理总局行政事项受理服务和投诉举报中心(简称受理和举报中心)10个工作日完成。
十六、申请人权利和义务
(一) 依据《中华人民共和国行政许可法》,申请人依法享有以下权利:
- 依法取得行政许可的平等权利;
- 对行政机关实施行政许可,享有陈述权、申辩权;
- 依法申请行政复议或者提起行政诉讼;
- 合法权益因行政机关违法实施行政许 可受到损害的,有权依法要求赔偿。
(二) 依据《中华人民共和国行政许可法》,申请人依法履行以下义务:
- 对申请材料实质内容的真实性负责;
- 依法开展取得行政许可的活动;
- 如实向负责监督检查的行政机关提供 有关情况和材料。
(三) 申请人应当履行《中华人民共和国药品管理法》《中华人民共和国药品管理法实施条例》等规定的相应义务。
十七、咨询途径
(一) 窗口咨询;
(二) 电话咨询;
(三) 电子邮件咨询;
(四) 信函咨询。
- 部门名称:国家食品药品监督管理总局食品药品审核查验中心
- 通讯地址:北京市东城区法华南里小区11号楼三层
- 邮政编码:100061
- 联系电话:010-87559000
- 电子邮箱:cfdi@cfdi.org.cn
十八、监督和投诉渠道
部门名称:国家食品药品监督管理总局行政事项受理服务和投诉举报中心
通讯地址:北京市海淀区莲花池东路39号西金大厦七层
邮政编码: 100036
电话:12331
十九、办公地址和时间
国家食品药品监督管理总局食品药品审核查验中心
办公地址:北京市东城区法华南里小区 11号楼三层
对外办公时间
上午9∶00—11∶30
下午13∶00—16∶00
二十、公开查询
可通过国家食品药品监督管理总局网站http://www.cfda.gov.cn或国家食品药品监督管理总局食品药品审核查验中心网站www.cfdi.org.cn查询审批状态和结果。
二十一、 实施日期
自2017年12月1日起施行。
附 录
填 表 说 明
一、资格认定申请内容的填写应准确完整,字迹清晰,不得使用没有规定的符号、代码和缩写。
二、隶属机构指上一级主管部门,无主管部门的可以空项。
三、机构所有制形式、医疗机构类型、经营性质和床位数填写应与《医疗机构执业许可证》中相一致。
四、申请认定专业名称:填写拟申请的 专业名称,Ⅰ期临床试验研究室按独立专业申请。
五、住院人数(人次/年)、门急诊量 (人次/日)填写近3年的。
六、如是选择项,请在所选择项相应的 中打 “√”。
七、电话和传真号码均应填写区位号。
八、初审日期由省级卫生厅(局)填写。
九、形式审查日期由省级食品药品监督 管理局 ( 药品监督管理局) 填写。
十、受理日期及受理编号由国家食品药 品监督管理局填写。
十一、报送申请表及电子软盘一式2份。