-
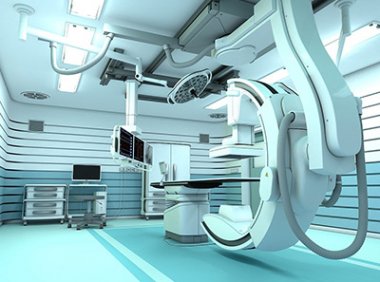
医疗机构临床急需医疗器械临时进口使用管理要求(2024年6月19日)
为规范医疗机构临床急需医疗器械临时进口使用管理,进一步满足临床诊疗急需,按照《医疗器械监督管理条例》(国务院令第739号)等相关规定,国家药品监督管理局会同国家卫生健康委组织制定了《医疗机构临床急需医疗器械临时进口使用管理要求》,现予发布,自发布之日起施行。...
- 1
- 0
- 1.6k
-
《境内第三类和进口医疗器械注册审批操作规范》国药监械注〔2021〕53号
境内第三类和进口第二类、第三类医疗器械(包括体外诊断试剂)注册审批(指产品注册、变更注册和延续注册)包括受理、技术审评、行政审批和批件制作四个环节,临床试验审批包括受理、技术审评、行政审批三个环节,变更备案包括受理和文件制作两个环节。国家药品监督管理局医疗器械技术审评中心对境内第三类和进口第二类、第三类医疗器械产品注册、变更注册、延续注册、临床试验审批项目进行技术审评,并提出技术审评意见。...
- 4
- 0
- 874
-
关于进口医疗器械产品在中国境内企业生产有关事项的公告解读
《公告》参考借鉴国际相关要求,结合我国医疗器械注册、监管、临床使用等方面的实际情况,基于医疗器械科学监管的原则,在产品设计不发生改变、质量体系保持基本一致,产品安全有效性没有发生显著变化的前提下,通过认可部分已注册进口医疗器械的原已提交的注册申报资料,从而优化相应审查资料要求,避免资料的重复提交。《公告》也明确境内企业和境外企业的一致性原则,对于境内企业投资境外企业并在境内企业生产同样适用。...
- 2
- 0
- 1.4k
-
国家药监局关于进口医疗器械产品在中国境内企业生产有关事项的公告(2020年 第104号)
进口医疗器械注册人通过其在境内设立的外商投资企业在境内生产第二类、第三类已获进口医疗器械注册证产品的有关事项,适用本公告。(一)进口医疗器械注册人在中国境内设立的外商投资企业作为注册申请人,向药品监督管理部门提交境内医疗器械注册申请。注册申请人按照相关要求提交注册申报资料。注册申报程序按照《医疗器械注册管理办法》《体外诊断试剂注册管理办法》以及医疗器械电子申报相关规定执行。...
- 2
- 0
- 1.1k
-
《境内第三类和进口医疗器械注册审批操作规范》食药监械管〔2014〕208号
境内第三类和进口第二类、第三类医疗器械注册审批包括受理、技术审评、行政审批和批件制作四个环节,登记事项变更包括受理和文件制作两个环节。受理和批件制作、登记事项变更由国家食品药品监督管理总局行政事项受理服务和投诉举报中心负责;技术审评由国家食品药品监督管理总局医疗器械技术审评中心负责;行政审批由国家食品药品监督管理总局负责。...
- 3
- 0
- 1.5k
-
医疗器械临床试验机构条件和备案管理办法(自2018年1月1日起施行)
为了加强和规范医疗器械临床试验机构管理,根据《医疗器械监督管理条例》的规定,制定本办法。本办法所指的医疗器械临床试验机构备案,是指医疗器械临床试验机构按照本办法规定的条件和要求,将机构概况、专业技术水平、组织管理能力、伦理审查能力等信息提交食品药品监督管理部门进行存档、备查的过程。...
- 2
- 0
- 4.1k